Aminoácidos
Los aminoácidos
son los monómeros de las proteínas. Químicamente están formados por un átomo de
C central o alfa que es quiral, excepto en la glicina. A este C se le unen un
H, un grupo amino -NH2, un grupo carboxilo -COOH y un resto hidrocarbonado -R,
que varía según el aminoácido, y es el que le otorga la polaridad o apolaridad
al aminoácido. A su vez, los polares se dividen en los que no tienen carga, y
los que tienen (positiva o negativa).
La presencia de grupos básicos (-NH2) y ácidos (-COOH) en la misma
molécula hacen que sean anfóteros, es decir, que según el pH del medio van a
estar cargados o no: a pH ácido con carga positiva (por el -NH3+); a pH
isoeléctrico van a estar neutros (-NH3+ y -COO-), que se anulan
las cargas) y a pH alcalinos van a estar con carga negativa (por el -COO-).
Existen 20 aminoácidos que conforman las proteínas en el organismo
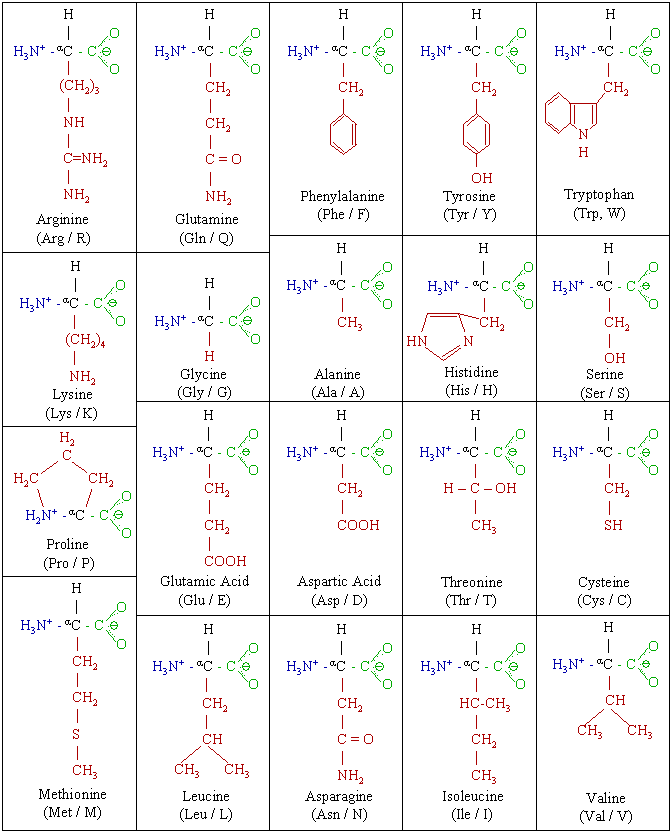
Estos aminoácidos se pueden clasificar de la siguiente manera
Alifáticos (no polares)
- Glicina (Gli) G
- Alanina (Ala) A
- Valina (Val) V
- Leucina (Leu) L
- Isoleucina (Ile) I
- Prolina (Pro) P
- Metionina (Met) M
Aromáticos
- Fenilalanina (Fen) F
- Triptófano (Trp) W
- Tirosina (Tir) Y
Polares cargados positivamente
- Lisina (Lis) K
- Histidina (His) H
- Arginina (Arg) R
Polares cargados negativamente
- Ácido aspártico (Asp) D
- Ácido glutámico (Glu) E
Polares sin carga
- Asparagina (Asn) N
- Glutamina (Gln) Q
- Treonina (Tre) T
- Cisteína (Cis) C
- Serina (Ser) S
También podemos clasificarlos en:
- Aminoácidos no esenciales: son aquellos que nuestro cuerpo puede fabricar por sí mismo y son: Arginina, ácido aspártico, cisteína, ácido glutámico, glutamina, glicina, prolina, serina, y tirosina.
- Aminoácidos esenciales: son aquellos que nuestro cuerpo no puede fabricar por sí mismo y, por lo tanto, necesitamos ingerir a partir de la dieta. Son: Histidina, isoleucina, leucina, lisina, metionina, fenilalanina, treonina, triptófano, valina y alanina.
pKa de los aminoácidos
Los aminoácidos tienen distintas estructuras de ionización y por tanto distintos pKa
Estructuras de ionización quiere decir distintas estructuras del mismo aminoácido en la cual una de sus partes ha sido ionizada por el pH.
Aminoácido
|
pKa1
-COO-
|
pKa2 -NH3+
|
pKa3 -R
|
Triptófano
(Trp) W
|
2.5
|
9.4
|
-
|
Glicina (Gli) G
|
2.4
|
9.8
|
-
|
Alanina (Ala)
A
|
2.4
|
9.9
|
-
|
Valina (Val) V
|
2.3
|
9.7
|
-
|
Leucina (Leu)
L
|
2.3
|
9.7
|
-
|
Isoleucina
(Ile) I
|
2.3
|
9.8
|
-
|
Lisina (Lis) K
|
2.2
|
9.1
|
10.5
|
Glutamina
(Gln) Q
|
2.2
|
9.1
|
-
|
Tirosina (Tir)
Y
|
2.2
|
9.2
|
10,5
|
Serina (Ser) S
|
2.2
|
9.2
|
-
|
Fenilalanina
(Fen) F
|
2.2
|
9.3
|
-
|
Asparagina
(Asn) N
|
2.1
|
8.7
|
-
|
Treonina (Tre)
T
|
2.1
|
9.1
|
-
|
Metionina
(Met) M
|
2.1
|
9.3
|
-
|
Glutamato
(Glu) E
|
2.1
|
9.5
|
4.1
|
Aspartato
(Asp) D
|
2.0
|
9.9
|
3.9
|
Prolina (Pro) P
|
2.0
|
10.6
|
-
|
Cisteína (Cis)
C
|
1.9
|
10.7
|
8.4
|
Arginina (Arg)
R
|
1.8
|
9.0
|
12.5
|
Histidina
(His) H
|
1.8
|
9.3
|
6.0
|

No hay comentarios:
Publicar un comentario